Pression de vapeur: notions de base et exemples
Qu'est-ce que la pression de vapeur ?
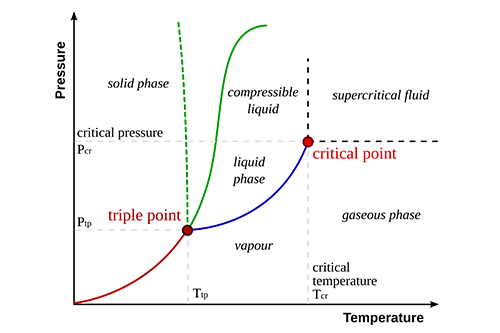
La pression de vapeur est la pression exercée par une vapeur en équilibre avec sa phase liquide ou solide à une température donnée. Elle indique la facilité avec laquelle une substance passe de l'état liquide à l'état gazeux.
Facteurs influençant la pression de vapeur
La température
Lorsque la température augmente, la pression de vapeur augmente car davantage de molécules ont l'énergie nécessaire pour s'échapper de la phase liquide.
Forces intermoléculaires
Des forces intermoléculaires plus fortes entraînent une pression de vapeur plus faible, car les molécules ont besoin de plus d'énergie pour se vaporiser.
Nature de la substance
Les pressions de vapeur varient d'une substance à l'autre en fonction de leur structure moléculaire et de leur liaison.
Mesure de la pression de vapeur
- Méthode manométrique: Un récipient scellé contenant un liquide est utilisé et la pression de vapeur est mesurée à l'aide d'un manomètre une fois que le système a atteint l'équilibre.
- Méthode dynamique: les changements de volume ou de poids du liquide sont suivis dans le temps pour calculer la pression de vapeur.
- Méthode par effusion: mesure la vitesse à laquelle les molécules de gaz s'échappent par un petit trou, ce qui permet de calculer la pression de vapeur.
- Équation de Clausius-Clapeyron: Utilisée pour calculer la pression de vapeur à différentes températures.
Importance de la mesure de la pression de vapeur
La mesure de la pression de vapeur est essentielle dans divers domaines, notamment
- Les prévisions météorologiques: La pression de vapeur est utilisée pour déterminer l'humidité et prévoir les schémas météorologiques.
- Les processus industriels: Elle aide à la distillation, à l'évaporation et à d'autres processus impliquant des transitions de phase.
- Génie chimique: Elle joue un rôle dans la conception d'équipements tels que les échangeurs de chaleur, les réacteurs et les évaporateurs.
- Produits pharmaceutiques: les mesures de la pression de vapeur sont importantes pour la stabilité et le stockage des composés volatils.
Exemples de pression de vapeur
L'eau
À 25 °C, la pression de vapeur de l'eau est d'environ 23,8 mmHg, ce qui indique une volatilité modérée.
Acétone
L'acétone présente une pression de vapeur plus élevée que l'eau à la même température, ce qui la rend plus volatile.
Mercure
La pression de vapeur du mercure est très faible, ce qui reflète ses fortes liaisons métalliques et sa faible tendance à se vaporiser.
Tableau des pressions de vapeur
Voici un tableau des valeurs de pression de vapeur pour diverses substances à différentes températures. La pression de vapeur est la pression exercée par la vapeur lorsqu'elle est en équilibre avec sa phase liquide (ou solide) à une température donnée.
|
Substance |
Pression de vapeur à 20°C (mmHg) |
Pression de vapeur à 100°C (mmHg) |
|
Eau |
17.5 |
760 |
|
Éthanol |
44.6 |
400 |
|
Acétone |
180 |
760 |
|
Méthanol |
95.3 |
1300 |
|
Benzène |
75.1 |
450 |
|
Éther diéthylique |
430 |
5800 |
|
Mercure |
0.0012 |
0.2 |
|
Hexane |
150 |
450 |
|
Toluène |
22.3 |
230 |
|
Chloroforme |
160 |
500 |
Pour plus d'informations, veuillez consulter le site Stanford Advanced Materials (SAM).
Questions fréquemment posées
Qu'est-ce que la pression de vapeur ?
La pression de vapeur est la pression exercée par une vapeur lorsqu'elle est en équilibre avec sa forme liquide ou solide.
Comment la température affecte-t-elle la pression de vapeur ?
L'augmentation de la température entraîne généralement une augmentation de la pression de vapeur, car davantage de molécules acquièrent l'énergie nécessaire pour se vaporiser.
Pourquoi la pression de vapeur de l'eau est-elle inférieure à celle de l'acétone ?
L'eau a des liaisons hydrogène plus fortes, ce qui nécessite plus d'énergie pour se vaporiser que l'acétone.
La pression de vapeur permet-elle de prédire la volatilité d'une substance ?
Oui, une pression de vapeur plus élevée indique une plus grande volatilité et une plus grande tendance à la vaporisation.
Quelle est l'importance de la pression de vapeur dans les prévisions météorologiques ?
La pression de vapeur contribue aux niveaux d'humidité, ce qui influence les modèles météorologiques et les précipitations.