Substrats, supports et ligands dans les catalyseurs à base de métaux précieux
Introduction
Les catalyseurs à base demétaux précieux sont largement utilisés dans diverses applications industrielles en raison de leurs propriétés catalytiques exceptionnelles. Toutefois, leurs performances sont fortement influencées par les matériaux auxquels ils sont attachés, appelés substrats, supports ou ligands. Ces matériaux jouent un rôle crucial dans la détermination de l'activité, de la stabilité, de la sélectivité et de la capacité de régénération du catalyseur. Voici un aperçu détaillé de ces composants et de leur importance dans les réactions catalytiques.
1. le substrat : Le fondement des réactions catalytiques
Le substrat est le matériau de surface sur lequel les métaux précieux sont fixés ou dispersés au cours des réactions catalytiques. Ceci est particulièrement important pour les catalyseurs hétérogènes. Le choix du substrat est crucial car il affecte la dispersion, la surface et l'activité catalytique des métaux précieux.
Les substrats les plus courants sont les suivants
- L'alumine (Al₂O₃) : L'alumine est connue pour sa grande surface et sa bonne résistance mécanique, ce qui en fait un choix populaire pour les substrats dans les réactions d'hydrogénation, d'oxydation et de reformage.
- Silice (SiO₂) : Les substrats de silice sont chimiquement inertes et très stables thermiquement, ce qui les rend appropriés pour les processus catalytiques nécessitant une grande sélectivité.
- Matériaux en carbone : Le carbone activé et les nanotubes de carbone offrent une excellente conductivité électrique et une grande surface, ce qui en fait des substrats idéaux pour les catalyseurs de piles à combustible et certaines réactions de réduction.
2. support : Améliorer les performances des catalyseurs
 [1]
[1]
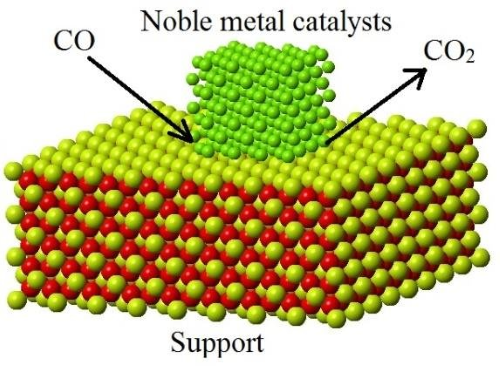
Les supports sont des matériaux utilisés pour disperser les métaux précieux à la surface du catalyseur, couramment utilisés dans les catalyseurs hétérogènes. La fonction première des supports est de fournir une surface élevée pour soutenir la dispersion des métaux précieux tout en stabilisant l'activité du catalyseur.
--Oxydes poreux
Les oxydes poreux tels que l'alumine, la silice et le titane sont appréciés pour leur surface élevée et leur stabilité, ce qui les rend idéaux pour disperser les métaux précieux.
- Alumine (Al₂O₃): Largement utilisée pour sa grande surface (100-300 m²/g) et sa stabilité dans les processus à haute température comme l'hydrogénation et le reformage.
- Silice (SiO₂) : Choisie pour son inertie et sa stabilité thermique (200-600 m²/g), elle convient aux réactions d'oxydation et au craquage catalytique.
- Titane (TiO₂) : Connu pour ses propriétés photocatalytiques, utilisé dans les processus activés par la lumière et le contrôle des émissions dans les applications automobiles.
--Supports en carbone
Lessupports en carbone, y compris le noir de carbone et le charbon actif, sont essentiels dans les applications électrochimiques en raison de leur conductivité et de leur grande surface.
- Noir de carbone : Il offre une excellente conductivité et est couramment utilisé dans les piles à combustible, où le platine sur noir de carbone (Pt/C) joue un rôle clé dans la réduction de l'oxygène.
- Carbone activé : avec une surface exceptionnellement élevée (500-1500 m²/g), il est idéal pour les processus d'adsorption et de filtration, soutenant efficacement des réactions telles que l'hydrogénation.
--Oxydes métalliques
Les oxydes métalliques tels que le cérium et la zircone présentent des propriétés d'oxydoréduction uniques, qui améliorent l'interaction avec les métaux précieux et renforcent l'efficacité catalytique.
- Ceria (CeO₂) : Efficace dans les réactions d'oxydo-réduction, en particulier dans les convertisseurs catalytiques automobiles, en raison de sa capacité de stockage de l'oxygène.
- Zircone (ZrO₂) : Connue pour sa stabilité thermique et sa robustesse dans des conditions difficiles, elle est couramment utilisée dans les processus d'isomérisation à haute température.
1) Ligands : Accorder les propriétés catalytiques
Les ligands sont des molécules ou des ions qui forment des liaisons de coordination avec le centre du métal précieux, principalement utilisé dans les catalyseurs homogènes. La structure et les propriétés des ligands ont un impact direct sur l'activité, la sélectivité et la stabilité du catalyseur.
Voici les types de ligands les plus courants :
- Ligands phosphine : Des composés comme la triphénylphosphine (PPh₃) sont largement utilisés dans les réactions de couplage croisé catalysées par le palladium, où ils régulent la sélectivité et la vitesse de la réaction.
- Ligands à base d'azote : Les ligands tels que la pyridine et la bipyridine peuvent ajuster la densité électronique des métaux précieux, influençant ainsi l'activité et la sélectivité de la réaction catalytique.
- Ligands chélateurs : Les ligands tels que l'EDTA peuvent former des chélates stables avec les métaux précieux, améliorant ainsi la stabilité du catalyseur, en particulier dans les réactions organiques complexes.
Facteurs influençant la performance des catalyseurs
La performance des catalyseurs à base de métaux précieux est déterminée par plusieurs facteurs associés aux substrats, aux supports et aux ligands.
- Surface et porosité : La surface et la porosité des substrats et des supports ont un impact direct sur la dispersion des métaux précieux et la disponibilité des sites actifs.
- Stabilité chimique : La stabilité chimique des supports et des ligands détermine la durabilité du catalyseur dans des environnements extrêmes, tels que des températures élevées ou des conditions fortement acides ou alcalines.
- Effets électroniques et environnement de coordination : Les propriétés électroniques et l'environnement de coordination fournis par les ligands peuvent grandement affecter les voies de réaction et la sélectivité du catalyseur.
Adaptation des catalyseurs à des applications industrielles spécifiques
Le choix des combinaisons de substrats, de supports et de ligands est souvent dicté par les exigences spécifiques des différentes applications industrielles. Ces matériaux doivent être soigneusement sélectionnés pour correspondre aux conditions de réaction et aux résultats souhaités.
Par exemple :
- Réactions d'hydrogénation: Les catalyseurs à base d'alumine sont largement utilisés dans les réactions d'hydrogénation en raison de leur surface élevée et de leur résistance mécanique.
- Piles à combustible : Les catalyseurs à base de métaux précieux soutenus par du carbone sont essentiels dans les piles à combustible, où une conductivité et une stabilité chimique élevées sont requises.
- Synthèse pharmaceutique : Les catalyseurs modifiés par des ligands sont souvent utilisés dans la synthèse pharmaceutique pour obtenir une sélectivité et une efficacité élevées dans des réactions organiques complexes.
|
Application |
Composant du catalyseur |
Matériaux clés |
|
Réactions d'hydrogénation Réactions |
Substrat |
Alumine (Al₂O₃) |
|
Substrat |
Silice (SiO₂) |
|
|
Piles à combustible |
Support |
Noir de carbone (Pt/C) |
|
Support |
Graphène |
|
|
Pharmaceutique Synthèse |
Ligand |
Modifié par la phosphine Palladium (Pd/PPh₃) |
|
Ligand |
Ligands chiraux (par exemple, BINAP) |
|
|
Oxydation Réactions |
Support |
Ceria (CeO₂) |
|
Support |
Titane (TiO₂) |
|
|
Reformage et |
Support |
Zircone (ZrO₂) |
|
Substrat |
Alumine (Al₂O₃) |
|
|
Polymérisation |
Support |
Ziegler-Natta (TiCl₄/MgCl₂) |
|
Support |
Métallocène (Silice/Alumine supporté) |
Pour plus de cas et d'exemples, veuillez consulter le site Stanford Advanced Materials (SAM).
Lecture connexe : Types de réactions courantes des catalyseurs homogènes à base de métaux précieux
Conclusion :
La sélection de substrats, de supports et de ligands appropriés est cruciale pour optimiser les performances des catalyseurs à base de métaux précieux. En choisissant soigneusement ces matériaux, il est possible d'adapter les propriétés du catalyseur aux exigences spécifiques des différentes applications industrielles, ce qui améliore l'efficacité et prolonge la durée de vie du catalyseur.
Référence :
[1] Hossain, Shaikh. (2018). Synthèse et étude cinétique des catalyseurs CuO supportés par CeO2 et SiO2 pour l'oxydation du CO. 10.13140/RG.2.2.31499.80165.

 Barres
Barres
 Perles et sphères
Perles et sphères
 Boulons et écrous
Boulons et écrous
 Creusets
Creusets
 Disques
Disques
 Fibres et tissus
Fibres et tissus
 Films
Films
 Flocon
Flocon
 Mousses
Mousses
 Feuille d'aluminium
Feuille d'aluminium
 Granulés
Granulés
 Nids d'abeilles
Nids d'abeilles
 Encre
Encre
 Stratifié
Stratifié
 Grumeaux
Grumeaux
 Mailles
Mailles
 Film métallisé
Film métallisé
 Assiette
Assiette
 Poudres
Poudres
 Tige
Tige
 Feuilles
Feuilles
 Cristaux simples
Cristaux simples
 Cible de pulvérisation
Cible de pulvérisation
 Tubes
Tubes
 Laveuse
Laveuse
 Fils
Fils
 Convertisseurs et calculatrices
Convertisseurs et calculatrices
 Chin Trento
Chin Trento



